PNAS丨王本课题组:人工构建细胞黏附受体调控细胞命运
2026年2月17日,浙江大学转化医学研究院/医学院附属第二医院王本教授课题组、浙江大学医学院附属第二医院胡新央教授课题组合作在美国科学院院刊PNAS上发表了题为“Artificially constructed collagen-targeting receptors on mesenchymal stromal cells promote anoikis resistance and tissue repair”的研究论文。
干细胞疗法在再生医学领域备受关注,其中间充质干细胞(MSC)因其来源广泛、分化潜能明确而备受关注。然而,由于其在病灶中的植入率和存活率较低,临床疗效仍然受限。
失巢凋亡(anoikis resistance)是指细胞因脱离细胞外基质而启动的一种程序性死亡,在肿瘤领域被广泛研究。在恶性肿瘤转移过程中,大多数循环肿瘤细胞会经历失巢凋亡,只有少数能通过适应性黏附重编程而存活并植入远端组织。乳腺癌相关研究显示,高表达E-cadherin的肿瘤细胞具有更强的转移能力,表明功能性黏附机制能够通过增强对失巢凋亡的抵抗来决定细胞命运。这一概念被延展到干细胞再生医学领域:能否通过增强干细胞的黏附能力,以帮助它们更好地“扎根”于损伤组织?
人体组织富含胶原,且不同的病理机制会触发不同的胶原改变。在心梗(MI)后,心肌组织会大量沉积以Ⅰ、III型胶原为主的纤维化基质;而在骨关节炎(OA)进展时,关节软骨中原本占主导的Ⅱ型胶原,会逐渐被以Ⅰ型为主、Ⅲ型为辅的纤维化基质所替代。血管性血友病因子(vWF)是一种重要的止血糖蛋白,能够通过与Ⅰ、III型胶原特异性互作在初始止血过程中发挥关键调节作用,在所有已报道的非细菌性蛋白质和多肽中,它表现出最强的胶原亲和力,其中A3结构域被确定为主要的胶原结合区域。
基于此,研究团队通过在MSC表面利用血管性血友病因子A3结构域(vWF A3)构建人工胶原靶向受体,从而提高它们在病灶中的植入和存活率。
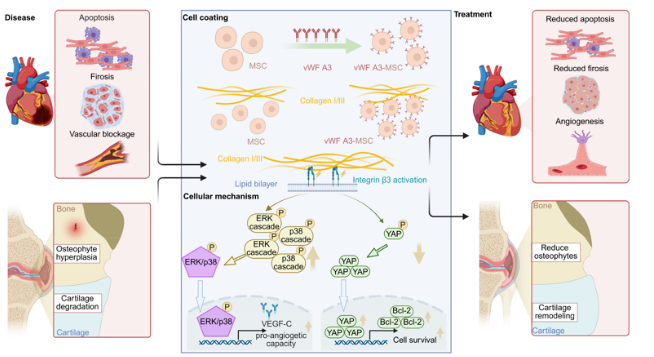
结合转录组测序、细胞因子检测等多种方法,研究团队揭示,vWF A3修饰不仅能提升MSC驻留率,还可增强细胞外基质-受体相互作用,激活整合素β3介导的信号通路,促进细胞的应激抵抗与促血管生成潜能,提升其在心梗和骨关节炎中的疗效。
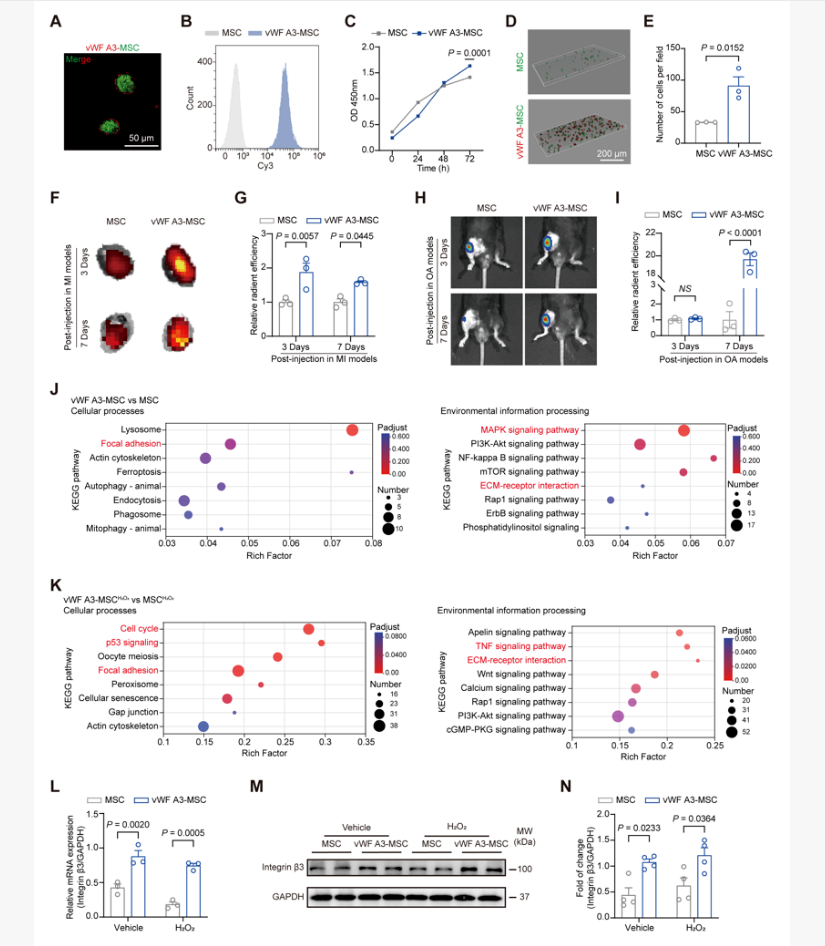
该项技术的开发,基于其“人源性”(低免疫风险)和“多功能”(集靶向、促存活、促修复多重功能协调)的优势,为多种纤维化、创伤修复疾病的通用型细胞治疗平台提供了全新思路。
浙江大学王本教授、胡新央教授为该文通讯作者。浙江大学徐迎回博士、陈源昊博士研究生、王亦琳博士研究生、杨泽博士为该文的共同第一作者。该项研究获得国家自然科学基金面上、重点项目和国家重点研发计划等经费资助。
文章信息:
Yinghui Xu#, Yuanhao Chen#, Yilin Wang#, Ze Yang#, Yating Ruan, Jianzheng Li, Yuqiao Huang, Xinliang Ming, Jing Zhao, Ying Zhang, Zhi Fang, Changchen Xiao, Xiaohui Zou, Xinyang Hu*, and Ben Wang*. Artificially constructed collagen-targeting receptors on mesenchymal stromal cells promote anoikis resistance and tissue repair. 2026, 123(8): e2525881123.
DOI: 10.1073/pnas.2525881123.
原文链接:www.pnas.org/doi/10.1073/pnas.2525881123


