Nat Commun│许军/李学坤合作发文:揭秘老药放线菌素D“拦截”致病基因转录,为儿童抗肿瘤药物改良及神经退行性疾病治疗开辟新途径
放线菌素D(Actinomycin D, ACTD)作为世界上首个获批临床应用的抗癌抗生素,自20世纪60年代起在临床沿用至今。在儿童肿瘤治疗中,ACTD是若干标准化联合化疗方案的重要组成部分,尤其用于肾母细胞瘤(Wilmstumor)和横纹肌肉瘤等疾病的治疗,但其毒性限制了临床使用。科学界已知ACTD通过嵌入DNA阻碍转录从而抑制癌细胞扩增,但其抑制真核生物核心转录机器——RNA聚合酶II(Pol II)的具体分子机制,在过去数十年中一直未能得到清晰的阐明。
2026年3月16日,浙江大学转化医学研究院/医学院附属儿童医院“百人计划”研究员许军课题组和李学坤教授课题组合作,在国际知名学术期刊《Nature Communications》(自然·通讯)上发表了题为“Stepwise transcription stalling by the anti-cancer drug Actinomycin D and insights into short tandem repeat transcription inhibition”(IF=15.7)的研究论文。该研究利用分子生物学与结构生物学技术,首次在原子水平上揭示了临床抗癌药物放线菌素D抑制RNA聚合酶II转录的动态全过程,并深入探讨了其在治疗短串联重复序列(STR)相关神经退行性疾病中的潜在应用价值。

(一)原子级视角:揭秘转录阻断的“三步走”
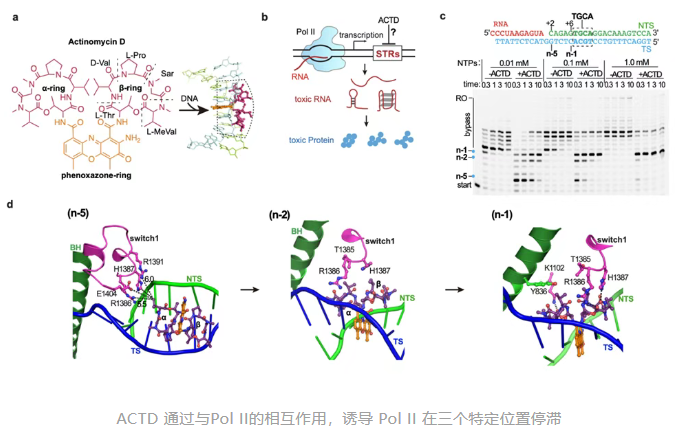
研究团队为系统阐明 ACTD 的作用机制,突破单一结构观察,建立了一个高度可控的体外转录重构体系,用于在实验条件下重现 Pol II的转录过程。该分子生物学平台构成了研究的关键实验基础。研究人员使用纯化的酵母与哺乳动物 Pol II,并在体外制备含特定 DNA 序列的模板,从而在可重复、可调控的条件下追踪 Pol II 穿越含 ACTD 的 DNA 区段时的行为变化。结果显示,ACTD 对转录的抑制并非随机发生,而具有明显的序列依赖性,并且在三个特定位置诱导 Pol II 出现停滞。
在此基础上,团队进一步采用冷冻电镜获取上述停滞状态的高分辨率结构信息。通过体外功能实验所揭示的停滞位点与冷冻电镜捕获的构象状态相互印证,从而在“功能—结构”两个层面共同勾勒出 ACTD 抑制 Pol II 转录的动态过程。值得注意的是,研究团队对比了酵母与牛(哺乳动物)的Pol II结构,证实了这一抑制机制在进化上高度保守,为药物的普适性应用提供了坚实的分子生物学依据。
(二)关怀患儿:优化临床用药的新希望
对于儿科临床医学而言,这项研究具有特殊的意义。ACTD虽然对儿童恶性肿瘤疗效显著,但其严重的毒性往往限制了临床剂量,甚至导致治疗中断。
许军研究员表示,“通过体外转录技术,我们可以系统地测试不同改造后的药物分子对转录效率的影响。结合蛋白质-药物相互作用细节,未来我们可以通过‘理性设计’对ACTD进行化学改造,开发出靶向性更强、毒性更低的第二代放线菌素,为患有实体瘤的儿童提供更安全、更有效的治疗方案。”
(三)针对神经系统疾病的新视野
除了癌症治疗,该研究还意外地发现ACTD在抑制“短串联重复序列(STR)”的转录方面具有巨大潜力。STR的异常转录与包括亨廷顿舞蹈症、强直性肌营养不良(DM1)在内的60多种神经系统疾病密切相关。
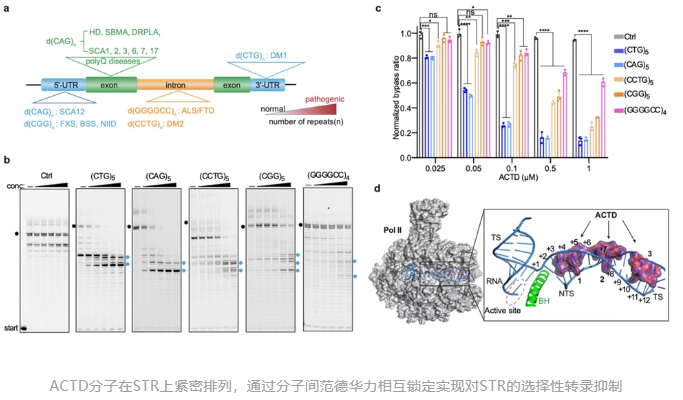
研究团队利用体外转录系统测试了五种疾病相关的富含GC的STR序列,发现ACTD能显著且选择性地抑制导致DM1的CTG重复序列和导致亨廷顿症的CAG重复序列。更具突破性的是,研究人员通过解析Pol II与多个ACTD分子结合的复合物结构,发现了ACTD分子间存在“协同效应”。在CTG重复序列中,多个ACTD分子可以像拼图一样紧密排列,通过范德华力相互锁定。这种协同结合极大地增强了药物在重复序列上的稳定性,意味着在较低浓度下即可有效阻断致病基因的转录。这一发现解释了为何ACTD在STR相关疾病模型中表现出优异的选择性,并为降低药物临床毒性提供了重要启示。
(四)展望:开启药物理性设计新篇章
尽管ACTD疗效显著, 但其临床应用受限于较高的毒副作用。本研究提供的原子分辨率结构图谱,为针对性地改造ACTD提供了“蓝图”。
通过深度学习等计算生物学手段,我们未来可以尝试对ACTD的肽链环进行精准修饰和改造,以增强其与Pol II或特定STR序列的相互作用, 同时减少对正常基因转录的影响,从而为抗肿瘤药物的改良以及神经退行性疾病的治疗开辟新途径。
该论文共同第一作者为浙江大学医学院附属儿童医院/转化医学研究院的博士研究生赵玮琦、朱柳莲。通讯作者为许军研究员和李学坤教授。该研究得到了国家自然科学基金、浙江省自然科学基金等项目的资助。
原文链接:
https://www.nature.com/articles/s41467-026-70612-y


